Пороки стекла, вызванные химическим взаимодействием (док)
Вопрос о химической устойчивости может рассматриваться только с точки зрения готовых изделий: при их переработке, хранении или применении. В подавляющем большинстве случаев наиболее актуальными являются нежелательные реакции стекла с водой. Дополнительное влияние могут оказывать и такие компоненты атмосферы, как углекислота, оксид серы, оксид азота, специальные продукты испарения или горения, сопутствующие производству.
Практически невероятно появление пороков при взаимодействии чистых сухих газов со стеклом; чтобы это все же произошло, требуется влага.
Возникновение пороков, являющихся следствием реакции стекла с твердыми веществами, наиболее вероятно в тех случаях, когда на стекле осаждаются пылевидная шихта или щелочные сырьевые материалы (например, сода) и воздействуют на него в присутствии влаги или же непосредственно, в ходе последующего отжига при высоких температурах.
Причины химической активности поверхности стекла
Закономерности изменения физико-химических свойств силикатных стекол могут быть логично объяснены на основании существующих концепций о структуре стекла. Одним из основных факторов, влияющих на свойства стекла, является степень связности кремнекислородного каркаса и активность иона кислорода в стекле. Оксид кремния (SiO2) существует в стекле в форме тетраэдров [SiO4] разных видов. Эти тетраэдры должны обладать различными свойствами, в зависимости от того, в каком количестве находятся в стекле оксиды щелочных (Ме2О) и щелочноземельных (МеО) металлов, поскольку мостиковый (двухсвязный) кислород отличается по свойствам от немостикового (односвязного) кислорода. Другими словами, свойства [SiO2]-тетраэдров должны зависеть от степени связности кремнекислородного каркаса. Мерой степени связности служит коэффициент fsi, равный отношению числа атомов кремния к числу атомов кислорода (Si / O), или обратная величина — кислородное число R = O / Si.
Коэффициент fsi вычисляют по формуле:
FSi = VSiO2 : (VМе2О + VМеО + 3VМе2О3 + 2VМеО2 + 5VМе2О3 + 3VМеО3)
Для структуры чистого кварцевого стекла, состоящего целиком из тетраэдров [SiO4], каждая из кислородных вершин является общей для двух соседних тетраэдров. Каждая молекула SiO2 состоит из одного иона кремния и четырех равноотстоящих от Si4+ половинок двухсвязных ионов кислорода. При введении в кварцевое стекло оксидов Ме2О или МеО одна вершина у части (SiO4)-тетраэдров “ослабляется”, т.к. по соседству с ионами кислорода оказываются ионы Ме2+,1+, обладающие более слабым полем, чем Si4+. Количество таких тетраэдров возрастает по мере увеличения содержания в стекле Ме2О и МеО. Этот процесс изменения структуры кремнекислородного каркаса и находит свое отражение на свойствах SiO2 в стекле, а следовательно, и самого стекла. От степени связности кремнекислородного каркаса зависит состояние структурного кислорода в стекле, его активность. По теориям Захариасена и Уоррена сетка тетраэдров SiO2 разрывается встраиванием ионов натрия или кальция, причем разрыв происходит по немостиковым ионам кислорода. В процессе формования стекла большое количество щелочных ионов оказывается на поверхности стекломассы. Эта “незанятая щелочь”, количество которой вследствие медленного отжига может увеличиваться (ионы Ме поступают из внутренних слоев стекла), а также “немостиковые” ионы кислорода являются главной причиной химической реакционной способности поверхности стекла. На рис. 1 относительные размеры кружков указанных ионов соответствуют приблизительно соотношению ионных радиусов.
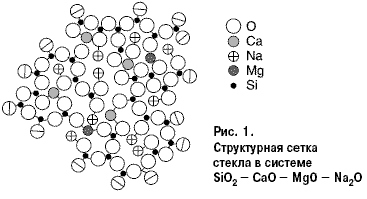
Восьмерная координация кальция, четверная — магния, включая два иона натрия, необходимые для уравнивания валентности, обозначены в виде роеобразования. Проекцией на плоскости каждый тетраэдр становится треугольником, каждый октаэдр — четырехугольником. Ионы кислорода, находящиеся на границе сетки, разделены пополам. Если представить себе, что правая граница схемы — поверхность, то видно, что при пяти молекулах кремнезема с немостиковыми ионами кислорода два щелочных иона энергетически готовы к химическому взаимодействию.
Принцип химического взаимодействия стекла при участии воды
Все химические изменения поверхностей стекла следует понимать, как реакции концевых элементов стекла с ненасыщенной валентностью, таких как кремний или координационно незанятые натрий и калий.
Для свежих поверхностей стекла, например, после его разрушения, мостиковая связь между ионами кремния нарушается, и образуются два различно заряженных нестабильных “радикала”:
![]()
Эти “радикалы” проявляют большую реакционную способность к молекулам среды, в которой они находятся, особенно воды:
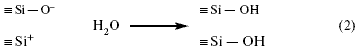
Это означает, что в обоих случаях атом кремния соединяется с группой ОН.
Реакцию (2) можно представить в следующем виде:
![]()
Группировку Si — OH называют силанол. Из реакции (2) можно проследить образование мостикового кислорода:
![]()
Силанольные группы химически реакционноспособны: ион водорода Н относительно легко передвигается (более подвижными являются щелочные ионы, связанные с кислородом, такие как натрий, литий) и может заменяться другими соединениями. На поверхности стекла могут таким способом появляться другие оксиды и при известных условиях целые слои. Затем адсорбируются молекулы воды, образуется состояние равновесия с водяными парами окружающей атмосферы. Химически связанный слой воды имеет толщину
10-10 см и называется “постоянный гидратированный поверхностный слой”, в противоположность “временному гидратированному поверхностному слою”, который адсорбируется физически равновесно в зависимости от содержания влаги в воздухе и имеет толщину приблизительно 10-7 см.
Химическое взаимодействие поверхности стекла с другими компонентами происходит всегда при участии воды или продуктов ее разложения:
![]()
Количественная связь этого уравнения дается константами равновесия по закону действующих масс:
![]()
Это означает, что в водном растворе концентрация ионов водорода Н+ должна увеличиваться, если концентрация ионов ОН– уменьшается, и наоборот.
Механизмы водной (гидролитической) и кислотной коррозии очень сходны: в обоих случаях происходит воздействие на катионы-модификаторы, особенно на реакционноспособные щелочные ионы.
![]()
Оба уравнения показывают, что ион натрия менее прочно связан с кислородом, чем ион водорода. На этом факте основаны процессы ионного обмена в водных растворах, известные как выщелачивание.
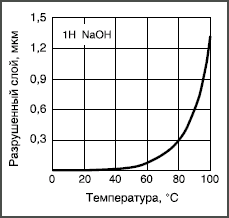
Рис. 2. Температурная зависимость растворимости боросиликатного стекла в 1 Н растворе NaOH.
Если гидролитическая и кислотная коррозия в обычных стеклах незначительна, то щелочные растворы сильно разъедают почти все стекла, растворяя даже их сетку. Интенсивность коррозии экспоненциально увеличивается с концентрацией щелочи и с температурой (рис. 2). Причина такой интенсивности щелочной коррозии заключается в том, что гидроксильные группы ОН могут расщеплять кислородную мостиковую связь между двумя ионами кремния:
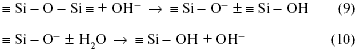
Здесь реагируют не возникающие группы, а разрушается внутренняя сетчатая структура, т.е. стекло растворяется. Например, кремнезем в щелочных растворах переходит в растворимый силикат, алюминий — в алюминат и т.д.
Пороки химического происхождения на поверхности стекла
Необходимо различать поведение водных сред при избытке и недостатке влаги. При недостатке воды (выделение конденсата) реакция возможна в момент появления влаги. В результате вполне вероятно превращение кислой среды, которая образовалась при адсорбции газов атмосферы (SO2 , CO2), в щелочную благодаря растворению в воде компонентов стекла по уравнениям (4) и (7).
Избыток воды
Только в этом случае на стекло воздействует именно вода, так как ее количество превышает количество продуктов реакции, которые к тому же отводятся от места реакции непосредственно после образования. Как уже отмечалось, по этой реакции “выщелачиваются” поверхностные слои стекол, т.е. в раствор переходят реакционноспособные и растворимые компоненты стекла. В первую очередь, это ионы щелочей. Двухвалентные ионы щелочно-земельных элементов реагируют существенно медленнее, т.к. алюминий и кремнекислота связаны с силикатным каркасом значительно прочнее.

Рис. 3. Гидролитическая обработка боросиликатного стекла в зависимости от времени.
Толщина выщелоченного слоя рассчитана из количества выделившегося Na2О.
Выщелачивание поверхности пропорционально времени t1/2. Графическое изображение зависимости количества выщелоченного материала от времени в начале имеет вид параболической кривой (рис. 3а). Если же на оси абсцисс отложить t1/2, то зависимость — прямолинейная (рис. 3б). При длительном гидролитическом воздействии устанавливается равновесие между поверхностью стекла и водной средой, и процесс растворения прекращается (рис. 4 и 5). Это является общей закономерностью процесса выщелачивания всех видов стекол, растворяющихся не полностью.

Рис. 4. Достижение равновесного состояния при выщелачивании калиево-стронциево-
силикатного стекла.
Приведены данные: о соотношении ионов K и Si, перешедших за сутки в раствор.

Рис. 5. Изменение состава в коррозионных слоях, обогащенных кремнекислотой
а — тонкий, но устойчивый слой;
б — толстый неустойчивый слой с меньшим содержанием SiО2
По завершении реакции с находящимися на поверхности щелочами взаимодействие переносится в нижележащие слои, преодолевая препятствие силикатной решетки, а следовательно, дальнейший процесс является диффузионным. Скорость диффузии при низких (примерно до 80°С) температурах сравнительно мала. В соответствии с уравнением (2), на поверхности образуются группы силанола. Этот процесс происходит тем интенсивнее, чем большее количество щелочей содержит стекло. Слой, образовавшийся в процессе реакций, при этом постепенно утолщается. Соответственно увеличиваются пористость и площадь поверхности. Такая поверхность способна адсорбировать воду и физическим путем в результате действия капиллярных сил, причем выщелоченные поверхностные слои разбухают. Они получили собственное название: слой геля кремнекислоты. С химической точки зрения они идентичны защитным слоям.
Если известково-натриевые или боросиликатные стекла используют в соответствии с их назначением, то на их поверхности образуется слой геля малой глубины, свидетельствующий о незначительности эффекта выщелачивания. В этом случае прозрачность стекла полностью сохраняется, а прореагировавший слой не виден без использования специальных оптических средств.
Слой геля толщиной до 100-200 нм можно увидеть невооруженным глазом: он отражает свет иначе, чем исходное стекло. Вследствие изменения показателя преломления уменьшается зеркальный эффект. На выщелоченном стекле появляются серые отпечатки. Однако до тех пор, пока поверхностный слой не представляет помех для нормального обзора, он еще не является пороком стекла.
При дальнейшем росте толщины выщелоченный слой становится белым и прозрачным; если же он достаточно порист, то выщелачивание может развиваться все глубже, слои будут отслаиваться, а стекло постепенно разрушаться (рис. 6).
Выщелоченная поверхность стекла способна присоединить ионы Cr (VI), Al (III) или Fe (III), которые благодаря своей окраске хорошо видны и не могут быть выделены даже водными растворами кислот. Если высушить слой кремнегеля, то выделится только физически адсорбированная вода, а химически адсорбированная остается связанной как постоянная водная оболочка (рис. 7).

Рис. 6. Стекло с сильно набухшими слоями: верху — нагрев слабее; внизу — сильнее

Рис. 7. Стекло, выщелоченное водой и ставшее “шероховатым” после прокаливания (поверхностная кристаллизация)
Если поверхность стекла взаимодействовала не с химически чистой водой (т.е. дистиллированной), а с обычной водопроводной, то при высушивании в осадке обнаруживаются следы примесей элементов, определяющих жесткость воды — карбонатов Са и Мg. Если такую поверхность подвергнуть высушиванию при 120°С, то примеси могут интенсивно реагировать со стеклом вплоть до образования пятен. Обычными способами очистки и даже кислотами удалить их не удается.
Недостаток воды
При наличии очень малого количества воды ход реакций в значительной мере изменяется. Однако стекло всегда может реагировать с влагой, присутствующей в атмосфере. Вода может выделяться и из сырого упаковочного материала (дерево содержит до 60% воды). Особенно серьезно это действие во влажном климате. На сильно охлажденных ночью листах стекла может выделиться конденсат. Как показано ранее, исходное гидролитическое взаимодействие с чистой водой переходит в щелочное. Поскольку ионы гидроксила действуют сильнее, чем молекулы воды, то по уравнениям (9) и (10) высвобождающиеся ионы OH– химическую активность повышают. Так как сильно щелочные растворы гигроскопичны, т.е. оттягивают на себя влагу, то из атмосферы могут поглощаться новые порции влаги. В результате адгезии воды могут образоваться тонкие щелочные пленки, оказывающие отрицательное воздействие на свойства поверхности. При переходе на щелочное воздействие разрывается кремнеземистый каркас, и стекло разрушается. При реакциях с недостатком воды речь идет, таким образом, о последовательном взаимодействии стекла с продуктами собственного разложения.
Грубые гидролитические пороки возникают, когда стеклоизделие, упакованное в бумагу или картон, хранят во влажной атмосфере. Упаковочный материал впитывает влагу и создает условия для начала гидролитических реакций. Нередко определенные составные части пропитки растворяются, ускоряя процесс. Типичное гидролитическое взаимодействие с влажным упаковочным материалом — так называемые отпечатки бумаги (рис. 8). Способы устранения таких пороков пока неизвестны.
Было отмечено интересное явление, когда между листами стекла распыляли тальк. С влагой он образует вид вяжущего, в результате выделения из стекла щелочей и кремнекислоты. Этот материал при комковании (например, из-за тряски при транспортировке) относительно крепко схватывается со стеклом (рис. 9) и формирует так называемые червеобразные образования, которые, впрочем, легко удаляются щелочными моющими средствами.

Рис. 8. Отпечатки бумаги

Рис. 9. Червеобразные образования на листовом стекле после просыпки стекла тальком
Наглядный пример гидролитической реакции, идущей при недостатке воды, — действие влаги, сконденсировавшейся между прилегающими друг к другу в стопе листами стекла, в результате чего в дальнейшем может образоваться порок. Расчет показывает, что при охлаждении 1 м3 воздуха, насыщенного влагой, с 35 до 25°С может выделиться 7,5 г воды. Капля воды массой 50 мг растечется по поверхности листа стекла на площади примерно в 50 см2 (при толщине слоя 0,05 мм). В этих условиях вполне могут происходить описанные ранее реакции, которые на первой стадии дают пятна разъедания. При определенных условиях они могут быть прозрачными. При длительном взаимодействии поверхностей стекла, сопровождающемся конденсацией, разъеданием, испарением и т.д., образуется соединение типа натриевого растворимого стекла:
![]()
В итоге этого процесса взаимодействие поверхностей стекол может быть столь интенсивным, что при попытке их разъединения стекло разрушится.
Потери стекла из-за склеивания имеют место в тех случаях, когда упакованные для длительного хранения или транспортировки листы стекла тесно соприкасаются. Сказанное поясняет кажущееся парадоксальным положение, что листовое стекло, абсолютно надежное в остеклении, оказывается в опасности в условиях длительного хранения в упакованном виде.
При гидролитическом действии с недостатком влаги (за большие промежутки времени) и взаимодействии с углекислотой воздуха вероятно полное извлечение СаО из стекла в виде растворимых гидрокарбонатов. Гидролитическое действие может быть уменьшено применением активных сред или благодаря образованию защитных слоев силикагеля. Это также может произойти, если в результате взаимодействия с атмосферой воздуха образуются новые соединения типа кальцита или гипса (СаSO4:).
Если после гидролитического действия при недостатке влаги продукты реакции отводятся из поверхностных слоев избытком влаги (дождь), то обычная гидролитическая реакция вызовет образование слоя геля кремнекислоты. Создается набухший слой, который вследствие колебаний температуры и влажности воздуха дегидратируется вновь и со временем, изменяясь химически и физически, достигает видимой глазом толщины, когда ее размер превышает 1/4 длины волны видимого света: тогда видны тонкие пленки, имеющие радужную кайму.
Окраска возникает вследствие явления интерференции видимого света на разрушенных поверхностных слоях. Первые признаки разрушения — слабое снижение светоотражения по сравнению с неразъеденной поверхностью, которое имеет легкую окраску (от серого до коричневого цвета). При дальнейшем утолщении слоя появляются, например, “голубые пятна” (рис. 11). По мере интенсификации гидролиза слой рассеивает свет сильнее и, наконец, становится белым. Большей частью он имеет вид облачного или пятнистого помутнения, а в экстремальных случаях слой может отслаиваться чешуйками.

Рис.10. Образование протравленного пятна между двумя листами стекла в результате возникновения на поверхности ионов гидроксила и, как следствие, образование щелочного раствора в месте
соприкосновения листов.

Рис. 11.
Голубые пятна на зеркальном стекле
Поверхностные гидролизованные слои состоят из силикагеля, который при отводе продуктов реакции непрерывно изменяется (внешний вид слоя аналогичен полученному при гидролитической обработке с избытком воды); если продукты реакции не удаляются, то они осаждаются или в толще слоя, или на его поверхности. Глубина пор в таком теле SiO2 составляет 50-120 A°. Наличие открытой структуры пор может быть доказано тем, что при внесении в слой красителей его цвет изменяется.
На рис. 12 показана примерная схема реакций стекла при недостатке воды, когда продукты реакции остаются на (или в) поверхностном слое.

Рис. 12. Схема взаимодействия стекла и влаги воздуха
(с водой в недостатке)
Особая форма разрушения листового стекла — так называемые нитяные кристаллы, или “воронья лапа”, которые образуются при реакции кислых оксидов воздуха (СО2 и SO2) со щелочами, высвободившимися при разложении стекла. Нитяные кристаллы состоят из карбонатов. Данные кристаллы, выросшие ориентированно в соответствии с направлением вытягивания стекла, показаны на рис. 13. Они появляются при условии, что стекло сначала увлажняется, а потом высыхает. Часто их можно наблюдать еще до первого помутнения. Они свидетельствуют о начале разложения, хотя еще и не являются дефектом поверхности стекла, а лишь предупреждают о возможности его появления.

Рис.13.
Нитяные кристаллы или “воронья лапа”, образовавшиеся в различных условиях взаимодействия стекла с оксидами воздуха (СО2 и SО2).
Избежать пороков типа “помутнения” и др. в промышленных масштабах можно путем использования растворов нитрата цинка при повышенных температурах (60-100°С). Такая обработка стекла должна более чем в 3 раза повысить устойчивость стекла по сравнению с необработанным.
Воздействие кислот
Избыток водных растворов кислот
Уравнение (8) характеризует процесс кислотного воздействия: замена ионов щелочных металлов с образованием силаноловых групп. Чтобы устранить, по мере возможности, выделение рассматриваемых ионов, например, из лабораторной посуды, которое может послужить серьезной помехой при выполнении аналитических работ, применяют способ выщелачивания посуды с помощью горячих кислот (“старение” лабораторной посуды).
Горячая концентрированная фосфорная и фтористоводородная кислоты способны разрушить стекло, воздействуя на него в любой концентрации, вследствие образования легко растворимых соединений с ионом кремния. Подобным же образом реагирует борофтористокремниевая кислота.
Химическое травление, преимущественно посредством растворов, содержащих плавиковую кислоту или щелочи, повышает и механическую прочность стекла благодаря устранению дефектов поверхности.
Воздействие газообразной среды
Следы кислых газов всегда возникают в той зоне, где сжигаются твердое топливо, горючие газы или мазут. Тяжелое топливо содержит заметное количество серы, которая при горении образует оксиды. Действию высоких температур подвергается каждое изделие из стекла с момента его формования, а также при отжиге. Щелочные ионы реагируют, прежде всего, со следами кислот и кислотными ангидридами печной атмосферы, особенно с оксидами серы и углекислотой. Реакция в присутствии следов влаги для SO2 может быть представлена следующим образом:

Этим путем образуются соли, создающие сернистый налет на поверхности изделий. Поскольку в этом процессе щелочи в поверхностном слое стекла нейтрализуются, то данный налет играет роль защиты поверхности при отжиге. Снижение доли мазута как топлива стекловаренных печей и переход на электрические печи отжига стекла исключают процесс образования сернистого налета.
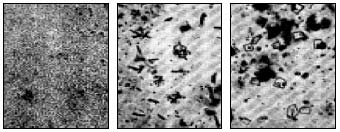
Рис.14. Микрофотографии сернистого налета в различных стадиях, закристаллизовавшегося под воздействием влаги воздуха
Газообразные продукты способствуют получению большей частью натриевых соединений на поверхности стекла, которые легко растворяются в воде. Поэтому данный налет на изделиях вообще не следует рассматривать как порок — его легко устранить промывкой водой. Сернистый налет может изменить свой внешний вид в результате перекристаллизации или гидратации, в частности, благодаря влажному воздуху; иногда для начала перекристаллизации достаточно той влаги, которая сообщается стеклу при прикосновении к нему рукой. На рис. 14 представлены микрофотографии сернистого налета, который закристаллизовался под действием влаги выдыхаемого воздуха.
Воздействие щелочей
В естественных условиях щелочные реакции возможны лишь тогда, когда ионы гидроксила, реагирующие при недостатке влаги, отбираются в соответствии с уравнением (11) и действуют как щелочи. Воздействие щелочей в избытке возможно лишь при специально создаваемых условиях.
Избыток щелочей
Под действием щелочей связи Si-O-Si кремнекислородного каркаса стекла разрушаются из-за реакций растворения, протекающих по уравнениям (9) и (10). С ростом температуры и концентрации ионов ОН- процесс усиливается вначале экспоненциально, позже — линейно (рис. 15). Указанный механизм имеет место при рН=10.
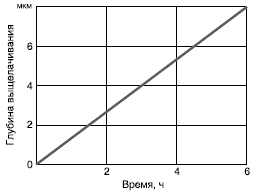
Рис. 15. Зависимость глубины выщелоченного слоя от длительности обработки боросиликатного стекла щелочами (1 N раствор NaOH, Т=100°C)
Такие реакции встречаются, когда первоначально нейтральная среда вследствие поглощения ионов ОН- становится щелочной. Этот случай уже подробно рассмотрен ранее.
Специфика химических взаимодействий поверхности флоат-стекла
Состав флоат-стекла и шихты, используемой для его варки, принадлежит к группе классических литых и тянутых стекол, для осветления которых обычно применяют сульфат натрия.
Контакт горячей стекломассы с расплавом олова и с восстановительной атмосферой в нормальных условиях не влияют на качество готового стекла, хотя состав поверхности стекла заметно отличается от основной его массы. Между имеющимися в составе стекла Na2SO4, а также содержащимся в защитной атмосфере флоат-ванны водородом (10%) и расплавом олова идут химические реакции с выделением летучих соединений: SnS, Na2S и H2O. В результате этих реакций поверхность стекла, обращенная к защитной атмосфере ванны, обедняется ионами Na+, Ca2+, Mg2+, (SO3)2–.
Вынос Na+ с поверхности, контактирующей с расплавом олова, облегчается тем, что в противодиффузии участвует некоторое количество олова в виде Sn2+. С обеих сторон ленты в очень сухую атмосферу флоат-камеры выделяется, кроме того, часть химически растворенной в стекле воды. Изменения состава ограничиваются толщиной поверхностного слоя стекла от 0,01 до 0,02 мм и зависят от продолжительности пребывания стекла во флоат-ванне, а следовательно, они увеличиваются с повышением толщины стекла. Различия в составе шестимиллиметрового стекла по толщине ленты приведены в таблице 1.
Таблица 1. Различие в химическом составе по толщине ленты флоат-стекла
| Стекло |
SiO2
|
Al2O3
|
Fe2O3
|
TiO2
|
CaO
|
MgO
|
Na2O
|
K2O
|
SO2
|
SnO2
|
| Верхний слой |
74.14
|
0.69
|
0.08
|
0.02
|
8.40
|
3.47
|
12.95
|
0.17
|
0.08
|
—
|
| Средние слои |
72.79
|
0.67
|
0.08
|
0.02
|
8.76
|
3.56
|
13.72
|
0.17
|
0.23
|
—
|
| Слои у расплава олова |
72.79
|
0.66
|
0.07
|
0.02
|
8.79
|
3.55
|
12.85
|
0.17
|
0.11
|
0.88
|
И.А. Кумалагов
Кандидат технических наук
Источник: http://oknamodern.ru/

